
[увеличи снимката] |
... | 
[увеличи снимката] |
Инфрачервени спектри могат да бъдат регистрирани в газообразно, течно и твърдо състояние. В зависимост от агрегатното състояние и използуваната техника за работа е необходимо различно количество от изследваното вещество. Задоволителни спектри се получават с 1-10 mg вещество без използуване на инфрачервен микроскоп и микропробна техника. Анализът е недеструктивен и изследваното съединение може да бъде използувано след измерването на спектъра за други цели.Регистриране (измерване) на инфрачервени спектри
1. Газообразни проби. Регистриране спектрите на газообразни проби е затруднено само в случаи на силно агресивни газове и пари. Най-често се работи при обикновено налягане, но има кювети за работа при високи и ниски налягания. Поради това, че в газообразно състояние веществата заемат много по-големи обеми отколкото в кондензирана фаза, се използуват кювети с голяма дебелина на работния слой. Към стандартното оборудване на спектрометрите е включена обикновено кювета с дължина 100 mm. Последната представлява стъклен (пирекс) цилиндър с кранове. Цилиндърът се затваря с прозорци от KBr или NaCl. Уплътняването на прозорците към цилиндъра става с каучуков пръстен. За изследване на ниски съдържания от газове и пари, например замърсявания на атмосферен въздух, се използуват многоходови газови кювети. Работната дължина при тях се увеличава чрез многократно отражение на лъча. Понастоящем фирмите предлагат газови кювети с дължина от 1 m до над 100 m. С такива кювети са били определени азотни окиси, СО, етилен и др. газове в атмосферен въздух в съотношение под 1 ppb (части на милиард).
Обичайният начин на работа се състои в евакуиране на газовата кювета с маслена вакуумпомпа и всмукване на анализирания газ. Тази процедура може да се повтори неколкократно ("промиване" на кюветата), с което се отделят адсорбираните по повърхността на кюветата газове, а освен това се осигурява по-добро запълняне.
При извършване на количествени определения анализираният газ се смесва с инертен газ, най-често азот. Добавката на инертен газ се използува в редица случаи и за повишаване интензитета на абсорбционните ивици на определяемия газ поради т.н. "ударно уширение".
2. Течности. Най-често използуваният
метод за регистриране на проби в течно състояние е т.н. капилярен
слой. Когато изследваното вещество е достатъчно вискозно, капка
от него се поставя между прозорците от KBr (или NaCl) и се подлага на фотометриране
- вижте фигура 1. В участъците, в които ивиците са прекалено интензивни,
спектърът се регистрира повторно след внимателно притискане на прозорците
за намаляване дебелината на слоя. При много вискозни проби се практикува
премахване на единия от прозорците чрез приплъзване и измерване спектъра
на веществото, останало по другия.
.

[увеличи снимката] |
... | 
[увеличи снимката] |
Фигура 1. Измерване в капилярен слой. В ляво - плочки от KBr и NaCl. В дясно - пробата межд две плочки в държателя, закрепен в гнездото на ИЧ апарат FT-IR Perkin-Elmer 1750.
Лесно летливи и невискозни проби се измерват
в кювети с дебелина от 5 до 25 mm
- вижте фигура 2. За такива дебелини е достатъчно поставянето на една капка
в единия от отворите на кюветата. За да се ускори запълването в срущуположния
отвор, се създава леко подналягане. След регистриране на спектъра кюветата
се измива неколкократно с разтворител, който също може да изсмуква с водна
вакуумпомпа. Сушенето на всички кювети след измиване става с въздух, преминал
през сушител, за да се избегне кондензация на влага по прозорците.
.

[увеличи снимката] |
... | 
[увеличи снимката] |
Фигура 2. Измерване в кювети. В ляво - кювета с прозорци от KBr с дебелина 0.01 mm (10 mm.). В дясно - кювета в гнездото на ИЧ апарат FT-IR Perkin-Elmer 1750.
Спектрите на някои природни вещества (восъци и др.) могат да бъдат регистрирани в стопено състояние. За тази цел прозорците заедно с веществото се загряват до стапяне на последното, притискат се и се поставят на пътя на лъча. Обикновено по време на регистриране на спектъра веществото не се втвърдява, понеже само по себе си инфрачервеното лъчение поддържа достатъчно висока температурата на пробата.
3. Разтвори. Молекулните трептения на веществата в кондензирана фаза са затруднени поради процеси на асоциация. За изследване трептенето на атомите в свободните молекули веществата се разтварят в подходящи разтворители. Последните трябва да отговарят на няколко изисквания: да не взаимодействат с веществото, да не кородират прозорците от KBr и NaCl, да няма много собствени ивици на поглъщане. Най-подходящи за инфрачервената спектроскопия са CCl4 и CS2, но те разтварят ограничен брой вещества. Приложение в практиката намират също CHCl3, C2Cl4, CH3Cl. Със силно полярни разтворители може да се работи само с кювети от CaF2 и КRS5. На фигура 3a е даден спектърът на хлороформ, а на фигура 3b - този на тетрахлоретилена.


Разтворителите притежават абсорбционни ивици, някои от които не могат да бъдат компенсирани, дори при дебелина на кюветата от 0.1 mm. Ето защо за получаване на пълен спектър на изследваните съединения е необходимо техните спектри да се регистрират в няколко разтворителя. Най-често това не се налага, тъй като обикновено спектрите преследват конкретна цел. В учебника за студенти [1] в таблица 3.10 на страница 122 са дадени областите на поглъщане на най-често използуваните в инфрачервената спектроскопия разтворители.
Обикновено разтворителите се подлагат на пречистване, сушене и дестилация преди работа. Дестилираният хлороформ се съхранява в хладилник, но не по-дълго от една седмица.
След продължителна работа повърхността
на кюветните прозорци помътнява, по тях се отлагат неразтворени вещества.
Кюветата се демонтира, прозорците се полират върху специална стъклена повърхност,
а след това върху плат или кожа. Ограничителният оловен пръстен, задаващ
дебелината на слоя се амалгалира преди монтиране на кюветата. След монтиране
се измерва дебелината на кюветата. Най-често за тази цел се използува интерференчният
метод, който е подходящ за кювети с дебелини от 25 до 70 mm.
Празната кювета се поставя на пътя на лъча и при сканиране се измерват
максимуми и минимуми, възникнали в резултат на отражение на лъчението от
вътрешните повърхности на прозорците. Разстоянието между прозорците, B
в mm, се определя по формулата:
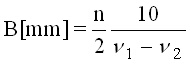 (1)
(1)където n е броят максимуми между вълнови числа n1 и n2.
4. Твърди проби. Най-често използуваните техники за регистриране на спектри в твърдо състояние са: таблетиране, суспендиране и директно измерване на ципи (фолии).
При таблетирането се използува свойството на KBr да дава при налягане и вакуум прозрачна за инфрачервената и видимата светлина таблетка. В далечната инфрачервена област за таблетиране се използуват полиетилен, полипропилен и тефлон.
Изследваната проба (0.5 до 2 mg) се смила
в ахатов хаван или вибрационна мелница с около 300 mg KBr в продължение
на 3-4 min., насипва се в матрицата, изравнява се повърхността с поасона,
включва се към маслена вакуум помпа и без да се спира евакуирането се създава
налягане от около 1000 kg/cm2 с маслена
преса. Ако фонът на регистрирания инфрачервен спектър нараства силно с
повишаване на вълновото число (ефект на Христиансен), таблетката се смила
повторно и процедурите се повтарят. Теоретически размерът на частиците
трябва да бъде по-малък от най-малката дължина на вълната, с която ще бъде
облъчвана пробата т.е. под 2.5 mm,
но на практика не се постигат такива резултати. Понякога смилането се извършва
в присъствие на подходящ органичен разтворител, но обикновено при изпаряването
му върху повърхността кондензира атмосферна влага.
.

[увеличи снимката] |
... | 
[увеличи снимката] |
Фигура 4. Измерване в таблетки от KBr. В ляво - пресата за формуване на таблетки, матрицата и ахатовия хаван. В дясно - поставяне на готовата таблетка в държателя.
KBr техниката има редица положителни страни: отсъствува собствено поглъщане (на KBr), пробите, необходими за работа са в значително по-малки количества, отколкото при разтвори и суспензии, може да се извършва количествен анализ. Основен неин недостатък е опасността от полиморфни превръщания и йонен обмен на изследваните съединения с KBr, както и деструкция на някои сложни органични съединения. Влагата, която дава ивици при около 3300 сm-1 и 1650 сm-1 трябва да се компенсира с таблетка от същото количество KBr в сравнителния лъч.
Суспендирането е най-предпочитаният метод за регистриране на инфрачервени спектри на твърди проби. Суспендиращият агент трябва да бъде инертен спрямо изследваните химични съединения и алкални халогениди, коефициентът му на пречупване да бъде близък до този на въздуха, да бъде безопасен за работа, да има значителен вискозитет и ниска летливост, да няма собствени ивици на поглъщане и пр. Най-главните от тези изисквания се удовлетворяват от парафиновото масло (нормални наситени въглеводороди със среден състав С25), наречен в практиката нуйол. Единственият недостатък на нуйола е наличието на собствени ивици на поглъщане. За доказване или отхвърляне на предположение за присъствие на -СН3 и - СН2- групи в дадена проба спектърът трябва да се регистрира в друг суспендиращ агент. За тази цел се ползуват следните химични съединения, в молекулата на които няма С-Н връзки: хексахлорбутадиен, флуоролаб (напълно флуориран керосин) и пердеутеронуйол (напълно деутериран въглеводород). На фигура 5 са представени инфрачервените спектри на нуйол и флуоролаб. Очевидно, за да се получи пълен спектър на изследваното съединение, то трябва да бъде измерено в двете суспендиращи среди (за да се избегнат участъците със силно собствено поглъщане на последните).
Приготвянето на суспензията се състои в разтриване на 5-6 mg от изследваното вещество с една капка суспендиращ агент в хаван или между шлифовани стъклени пестици, докато се получи равномерно разпределение на веществото. Кремообразната суспензия се изтъргва от пестиците с бръснарско ножче и се нанася върху единия прозорец. Вторият прозорец се поставя върху суспензията с леко приплъзване, за да се получи равномерен слой без мехурчета. Прозорците, със суспензията между тях, се поставят на пътя на лъча без предварително да се притискат силно. Ако някоя от ивиците на изследваното съединение се окаже с много висок интензитет, неразделена, е възможно дебелината на слоя да се намали чрез застягане с държателя.
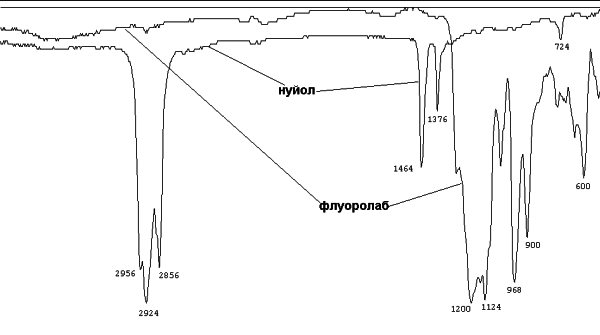
Фигура 5. ИЧ спектри на нуйол и флуоролаб, измерени в капилярен слой между плочки от KBr.
Ципи (фолии) от високомолекулни съединения с дебелина от 5-25 mm се регистрират директно. Понякога се явяват силни интерференчни ивици, чрез които може да се определи дебелината на фолиото. За премахване на интерференчната картина ципите се намазват с нуйол или се надраскват. Възможно е високомолекулното съединение да се разтвори в подходящ разтворител и да се излее върху повърхност - директно върху прозореца от алкален халогенид или върху стъкло. След изпаряване на разтворителя пробата се фотометрира директно или ципата се отделя от стъклото и измерва. Някои високомолекулни съединения се регистрират след нарязване или стриване чрез KBr-техника.
Автор: Проф. дхн Георги Андреев
Снимки и спектри: д-р Пламен Пенчев, Василия Митева