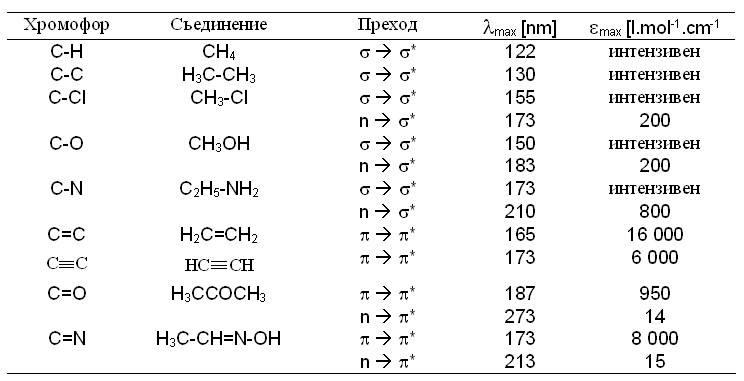
1. Абсорбция на изолирани хромофори. В направените в предишната лекция разглеждания се вижда, че положението и интензитетът на абсорбционни ивици зависи от природата на съответните електронни преходи. Поради голямата разлика в енергиите на свързващите и антисвързващите s - орбитали (фиг. 4 от част 2), за извършване на тези преходи е необходим квант от вакумният ултравиолет. Енергията на кванта, необходим за извършване на един pаp* преход е значително по-ниска, но все още е на границата между далечната и близка УВ област. И при двата случая преходите са разрешени (N а V преходи), поради което съответните ивици имат висок интензитет. Някои примери на N а V преходи (а също на nаs* и n аp* преходи) са дадени в таблица1.Електронна спектроскопия
Част 3
Електронни спектри на някои хромофори
Таблица 1. Някои абсорбционни преходи
в изолиран хромофор.

От таблица 1 се вижда, че на nаs* и n аp* преходите съответствуват слабоинтензивни ивици (N а Q преходи), проявяващи се на границата между далечната и близка ултравиолетова област. Следователно съединенията с прости връзки, дори в случаите, когато имат в молекулата си хетероатом, могат да се използуват като разтворители в електронната спектроскопия.
Ако при дадена молекула има заети повече от една s, p или n-орбитала, които не взаимодействуват помежду си, следва да се очаква електронният спектър да бъде суперпозиция от ивиците на единичните хромофори. Наличието на стерични ефекти, пръстенно напрежение и др. водят до пространствени сближавания, които са причина за поява на взаимодействия. В резултат на тези взаимодействия положението на ивиците се променя, а понякога последните се разцепват. Например 1,4-пентадиенът, който е неспрегнат, притежава ивица с максимум при дължина на вълна при 178 nm и emax = 17,000 [l.mol-1, cm-1],

докато норборнадиенът има две ивици със
сложна структура с максимум при 205 nm и рамо при 230 nm. Причина за тази
разлика в електронните абсорбционни спектри на тези две съединения е взаимодействието
между двете двойки връзки в норборнадиена, които са подходящо пространствено
разположени, за разлика от тези в 1,4-пентадиена.
2. Абсорбция на спрегнати двойни връзки. Спрегнатите хромофори имат най-голямо значение за органичната химия, понеже абсорбционните ивици лежат в близката ултравиолетова и видима област.
В таблица 1 са дадени характеристиките на pаp* преходи при неспрегната двойна връзка. Ако етиленовата двойна връзка бъде спрегната с втора етиленова двойна връзка в образуваната бутадиенова система, енергетичните нива се разцепват две по две. Бутадиенът има четири електронни молекулни орбитали, двете от които са свързващи, другите две - антисвързващи - фигура 2..
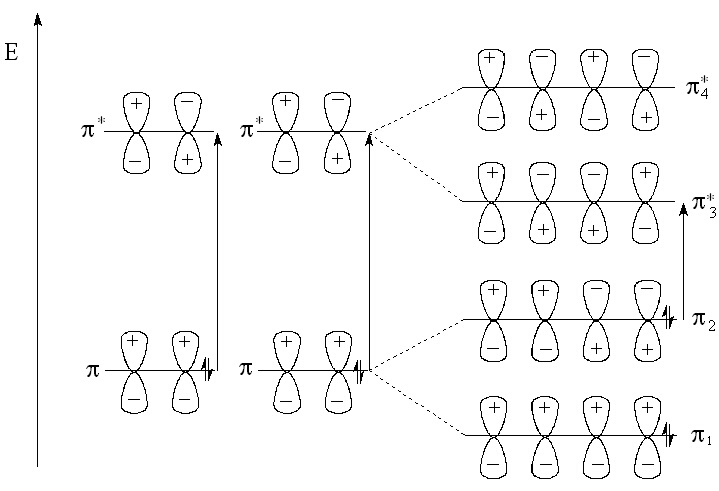
От фигурата се вижда, че енергетичните разлики между най-високата заета молекулна орбитала в бутадиена (НОМО) и най-ниската незаета орбитала (LUMO) се намалява в сравнение с етилена. Това е причина за намаляване на енергията на светлинния квант, необходим за извършване на преходи т.е. абсорбционният максимум на прехода се премества батохромно при спрежение. Наред с това нараства интензитетът на ивицата. Ако броят на спрегнатите двойни връзки надхвърли пет, абсорбционната ивица се проявява над 350 nm и съединението е вече цветно - таблица 2.
Таблица 2. Дълговълнови абсорбционни
ивици в спрегнати полиени от вида CH3-(CH=CH)n-CH3.
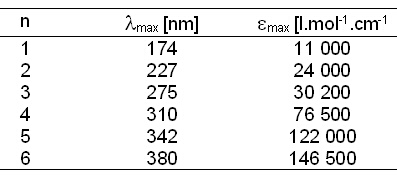
К-ивиците на полиените не променят положението си под влияние на вида на разтворителя. В неполярни разтворители тази ивица има фина структура поради електронно-вибрационно взаимодействие. Разликата между честотите на отделните линии, съставящи ивицата, е около 1600 см-1, което отговаря на честотата на валентните С=С трептения.
За електронните спектри на полиините са характерни две ивици в близката УВ област, които проявяват фина структура с разстояние между отделните вибрационни максимуми от около 2000 см-1. Последната стойност се различава от онази при полиените, което би могло да бъде използувано за отличаване на двата типа спрегнати системи.
К-ивицата в полиени и циклични системи с четен брой атоми проявява интересна особеност: положението на абсорбционния максимум зависи единствено от броя на спрегнатите двойни връзки - вижте таблица 3.
Таблица 3. Абсорбции на спрегнати
полиени с участие на различни атоми.

Както се вижда от данните в таблицата, дължината на вълната на абсорбционния максимум остава практически постоянна за съединенията с една и съща спрегната система, независимо от разликата в електроотрицателностите на участвуващите атоми.
С увеличаване броя на двойните връзки се
засилва влиянието на вида на конфигурацията върху късовълновия преход при
спрегнатите полиени. Например ивицата при 340 nm в цис-b-каротена
отсъствува при транс-конфигурацията поради симетрична забрана (вижте предната
лекция). Симетрията в цис-заместеното съединение се нарушава и преходът
става разрешен (обертонова цис-ивица при каротените).
3. Бензен и производни. Пресмятанията на бензена с метода на МО на Хюкел водят до извода, че четири от неговите енергетични нива са две по две изродени. В експериментално измерените спектри се наблюдават три ивици при следните дължини на вълните: 180 nm (25,000), 200 nm (8,000) и 256 nm (230). Съгласно направената в предната лекция класификация само първият от тях е разрешен, докато останалите са забранени. Сравнително високият интензитет на ивицата при 200 nm, наречена К-ивица, се обяснява с известно "преливане" на интензитет от близколежащи разрешени ивици.
К-ивицата на бензена, заедно с най-нискочестотната (256 nm), наречена В-ивица, представляват интерес за органичната химия. В-ивицата притежава фина структура, която се запазва и при спектрите на бензен, заснети в разтвор. Ниският интензитет на тази ивицата показва, че преходът е забранен. Молекулата на бензена е високосиметрична и преходът v"0 а v'0 (фигура 3) не е свързан с промяна на симетрията (забрана по симетрия).
Ако дължината на една от С-С връзките в бензена се промени, симетрията се понижава и преходът става частично разрешен. Следователно ако една молекула бензен получи фотон, енергията на който е равен на разликата в енергиите на основното и възбудено електронно ниво плюс енергията на трептене на дадена връзка (преход v"0 а v'0), този фотон ще бъде погълнат. На фигура 3 е представен УВ-спектър на бензен, заснет в газово състояние. Всяка от тесните ивици ще съответствува на преход, представляващ комбинация от електронен и вибрационен преход на възбудено електронно състояние.
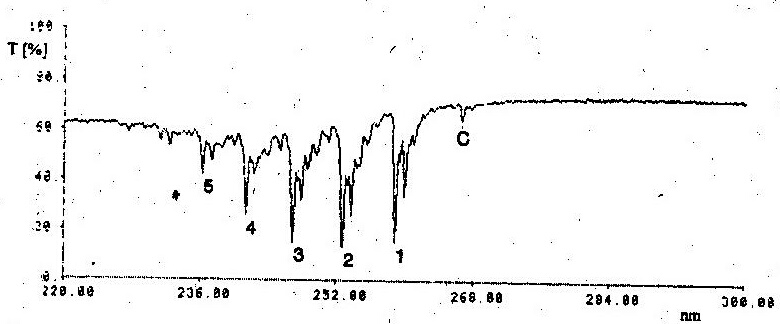
Чисто електронният преход v"0а v'0 е забранен и не се наблюдава в спектрите, а се пресмята теоретично (38,089 см-1). Ивиците с най-висок интензитет от всеки мултиплет (1,2,3...) имат вълнови числа, равни на сумата от забранения 0а0 преход и комбинация от трептения с вълнови честоти na = 520 и nb = 923 сm-1, които имат следните форми:
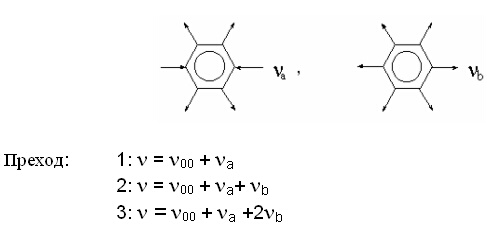
От изложеното следва, че изследвайки фината структура на вибрационните ивици на бензола и неговите производни можем да получим информация за трептенето на атомите във възбудено електронно състояние.
Известен брой молекули са населили още при стайна температура първото възбудено вибрационно ниво на основното електронно състояние. Преходът от това ниво v" = 1 до нулевото вибрационно ниво на възбуденото електронно състояние (v' = 0) е разрешен. Съгласно изложеното по-горе, той ще се проявява при вълново число с 608 см-1 по-ниско от това на v"0а v'0 прехода (ивица C на фигура 3).
Спрягането на бензена с кратна връзка води до батохромно отместване на К- и В-ивиците, като ефектът е почти еднакъв, независимо от електроотрицателността на атомите, образуващи връзката - таблица 4.
Таблица 4. Абсорбция на B- и К-
ивиците на бензола при спрягане с двойна връзка.

В спектрите на бензеновите производни,
наред с К и В-ивиците, се наблюдава и дълговълнова ивица на заместителя
(напр. при карбонилните съединения тя е около 330 nm). Причина за това
е p-p
спрягането на електронните двойки на ауксохрома с бензеновия хромофор.
Ако електронната двойка бъде блокирана (напр. в кисела среда), системата
проявява абсорбционен спектър както при съответния алкилбензол.
Фина структура на В-ивицата се наблюдава не само за бензен и негови производни, но и за други ароматни системи (пиридин, трополон и др.).
При спрягане на бензеновото ядро с ненаситени връзки неговите ивици претърпяват значително батохромно отместване, което се приписва на вътрешномолекулен пренос на заряд.
4. Полифенили. Електронните спектри на полифенилите зависят от мястото на свързване на бензеновите ядра. В спектрите на пара-полифенилите се наблюдават последователно батохромно отместване на абсорбционните максимуми с увеличаване броя на бензеновите ядра n и хиперхромен ефект.
За разлика от пара-, в спектрите на мета-полифенилите, спрежението при които се разпространява само между непосредствените съседи, абсорбционният максимум не променя положението си и спектрите им не се различават от този на бифенила. Наблюдава се само нарастване на интензитета с всяко ново бензеново ядро.
5. Полициклени въглеводороди. Абсорбционните спектри на линейните полициклени въглеводороди имат три ивици, както при бензена, които проявяват фина структура. Най-нисък интензитет имат В-ивиците, които се означават като a-ивици; К-ивиците се означават като р-ивици, а най-късовълновите - като b. С увеличаване броя на бензеновите ядра интензитетът на a и р-ивиците нараства, а абсорбционните максимуми се преместват към видимата част на спектъра. фигура 4. Първите три члена (бензен, нафталин и антрацен) са безцветни, но следващите са вече цветни съединения: тетраценът - жълтооранжев, пентаценът - синьовиолетов, хексаценът-тъмнозелен.
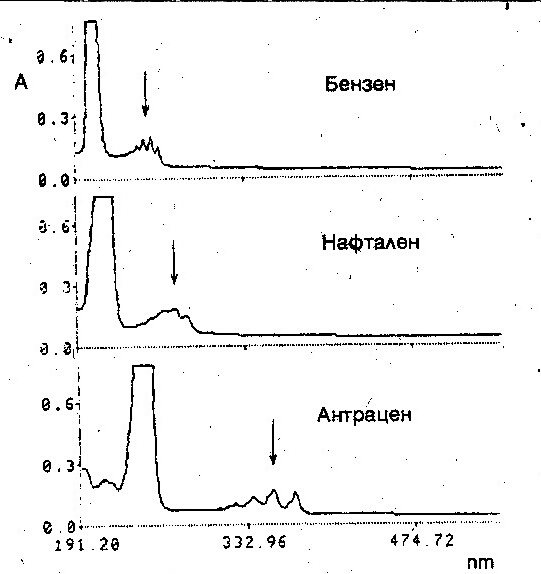
При ангуларно кондензирани полициклени въглеводороди увеличаването на броя на ядрата води до батохромно отместване на ивиците, но то (отместването) е по-малко, отколкото в съответните линейно кондензирани със същия брой ядра.
Едни от първите съединения с доказан канцерогенен ефект са ануларно кондензираните полициклени съединения 3,4-бензпирен, 1,2-бензпирен и др. Електронните спектри на тези съединения се използуват за качественото и количествено им определяне.
6. Абсорбция на ароматни хетероциклени съединения. р-p спрягането на електронната двойка от хетероатома и диеновата система в пирол, фуран и тиофен е причина за проявявания от тях ароматен характер.
Пиролът и фуранът имат абсорбционна К-ивица, положението на която (около 270 nm) е близко до онова на циклопентадиена.Тази ивица е най-дълговълнова и с най-нисък интензитет при тиофена lмах= 235 nm (7,000), което е в съгласие с неговия най-ясно изразен ароматен характер (бензен: 255 nm (260)).
Замяната на въглероден атом от бензеново ядро, нафтален, антрацен и др. с азотен атом води до незначителни промени на честотите на абсорбционните ивици, но до чувствителни промени на техния интензитет. Причина за това е нарушаването на симетрията в молекулите на пиридин, хинолин, акридин и др.
Литература
.
Автор: Проф. дхн Георги Андреев